
姓名:杨烁(Shuo Yang)
职称:青年研究员(Assistant Professor/Principle Investigator)
职务:研究组长(PI)
电子邮箱:shuo@fudan.edu.cn; lmys2356@live.cn
办公地点:上海市杨浦区淞沪路2005号,幸福宝导航app入口C521(School of Life Science, Fudan University, Room C521)
办公电话:021-31246738
课题组主页:https://lmys2356.wixsite.com (VPN)
研究方向:
从单细胞动物发展到多细胞动物,是动物进化史上的一个飞跃。从多细胞动物开始,动物身体的各个部分为适应外界环境而逐渐分化为具有特定功能的器官。经典理论认为,各器官的功能受到内分泌系统和神经系统的调控。而近些年的研究发现,除了神经/激素调控之外,不同器官之间可通过代谢小分子和非激素类分泌性蛋白实现相互调控,这种调控机制被称为信号的跨器官传递(Inter-organ communication networks, ICN)。ICN可以主动/被动响应多种病理变化,参与调控并维持机体器官正常生理功能和整体稳态。例如,ICN异常,与心脏瓣膜病、非酒精性脂肪肝、慢性肾炎等多种疾病的发生息息相关。因此,解析ICN,不仅可以增强我们对生命体器官间调控网络的认知,更可以为介入治疗系统性炎症风暴、神经损伤、肌无力等ICN相关疾病提供依据。特别的,ICN研究对模式动物多器官协同遗传操作的可行性和便捷性提出了很高的要求。借助于果蝇的遗传学操作优势,本人成功解析了天然免疫通路“肠-肝”之间的时空传递机制,以及依赖于“外胚层-肌肉”跨器官信号的肌肉发育双重调控网络。本人的研究为深入探索器官间调控网络,建立维持多器官稳态的分子图谱,阐发系统性炎症的治疗策略,解析遗传性肌肉疾病的致病机理等,提供了完善的理论支撑,并为今后工作提供了成熟的平台和研究策略。
一、解析天然免疫信号“肠-肝”传递的分子机制
肠道作为屏障系统,是机体抗击感染的第一道防线。研究表明,在肠炎进展过程中,一方面机体会直接响应感染,在肠道内激活局部免疫反应(Nature Microbiology, 2017);同时,也会通过活性氧-一氧化氮(ROS-NO)通路,将感染信号经血细胞(对应人体巨噬细胞)传递给远端的脂肪体(对应人体肝脏),从而激活系统性免疫反应。这种由局部免疫系统评估病理或生理损伤,从而警示并调节系统性免疫应答的机制,对于机体的免疫稳态维持和健康具有重要的意义。对该通路的研究一直集中于上游肠道内信号,而血细胞是如何接收并向下游器官转导信号,一直是一个悬而未决的问题。为了解答该问题,本人构建了果蝇天然免疫信号“肠-肝”传递模型,并证明了细菌感染和无菌肠炎,均可诱发天然免疫信号的“肠-肝”传递,这提示了该现象是一种普遍性的免疫机制。为了探索“肠-肝”传递的完整ICN通路,本人中采用血清质谱和代谢组学结合的策略,发现肠道局部免疫反应的激活,显著促进了血细胞中糖醇醛缩酶(Aldose Reductase,AR)的表达水平。AR作为机体平衡糖类和糖醇类稳态的核心代谢通路的限速酶(多元醇通路),其分泌至血清中后,即通过多元醇通路将血清中葡萄糖代谢为葡萄糖醇。随后,血清中升高的糖醇信号,作为第二信使,促进肝脏中金属蛋白酶Mmp2的表达和激活。激活性Mmp2则通过切割IMD通路受体PGRP-LC胞外结构域,最终启动系统性免疫反应(图1,通路①)。该研究从时间和空间上精确描述了天然免疫信号的“肠-肝”传递,并利用多种组学和遗传学手段,确定了一条并从酶、代谢分子、作用分子到免疫通路受体的完整ICN通路(Cell Host&Microbe, 2019)。
该项研究不仅精细地描述了天然免疫通路“肠-肝”之间的时空传递过程,而且定位了多元醇通路的糖醇小分子可以作为自身的警示因子(DAMPs/ALARMINs)。多元醇通路作为糖代谢的一种分支,在细菌感染,丙肝或糖尿病病人中常伴随慢性炎症的持续发生而上升。该研究表明,多元醇不仅调节炎性过程中糖代谢能量的产出,而且参与炎症反应中的信号传递,是免疫-代谢转换的枢纽。该研究深入揭示了多元醇在天然免疫通路时空调节中的重要作用,为今后干预系统性炎症提供了新视角和理论依据。
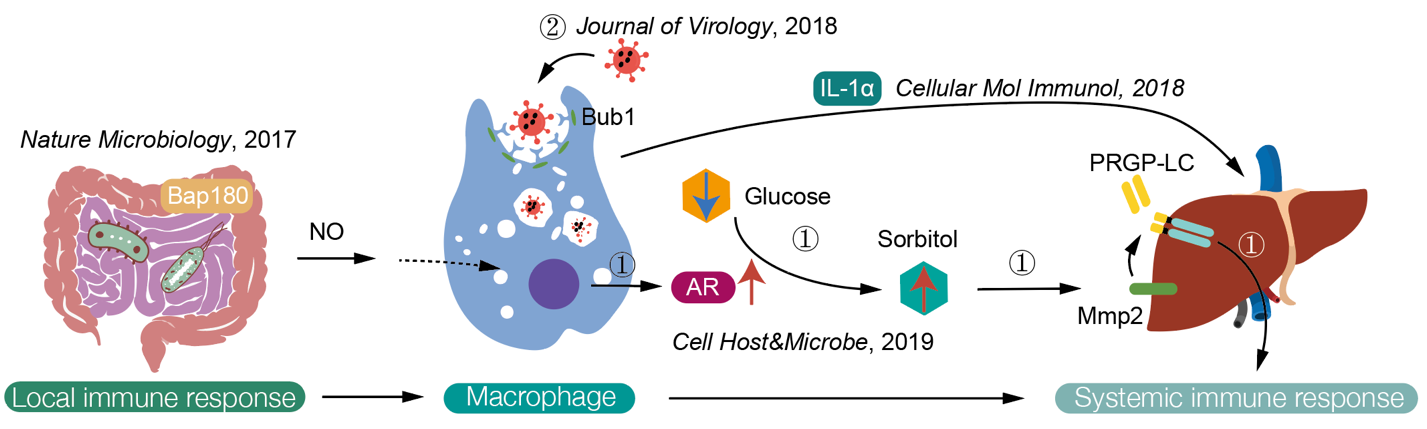
图1 天然免疫信号的“肠道-肝脏”传递
二、解析病原对宿主ICN系统的反制机制
机体进化出了局部免疫-系统性免疫的ICN预警系统,相应的,病原也伴随着进化出针对天然免疫ICN预警系统的反制机制。为了研究病原突破肠道等屏障系统后对宿主的影响,本人建立了基于多种病原的果蝇外伤性感染模型。利用该模型,综合相应遗传学手段,本人筛选并鉴定出一个重要的宿主保守因子Bub1,该分子可被人类病毒VSV (Vesicular Stomatitis Virus),李斯特菌(Listeria monocytogenes),以及果蝇病毒DCV (Drosophila C Virus)等所劫持(Journal of Virology, 2018)。进一步实验证明,Bub1通过与AP-1-2组分相互作用,参与一般性的内吞过程,而VSV等病原正是通过借助该过程促进自身对宿主细胞的侵染,破坏巨噬细胞功能(图1,通路②)。该研究表明,Bub1可以作为限制病原感染宿主的关键节点,为今后抗病毒药物靶点的开发提供了重要的理论依据。该论文发表后,本人被Jove出版社约稿撰写了关于果蝇病毒感染模型的方法性文章(Journal of Visualized Experiments, 2019)。近年来,随着甲流、登革热、寨卡以及新冠等病毒性传染病的爆发,如何治疗并防治病毒性传染病,是我国社会亟需解决的重大问题。一方面,昆虫作为中间宿主,可介导登革热、西尼罗河热等多种流行病的传播;另一方面,果蝇作为模式动物,是研究寨卡病毒、流感病毒等传染病的高效模型。果蝇作为传统遗传学模型,利用其丰富的遗传学工具,其不仅能够便捷的研究人类病毒/宿主相互作用,从而筛选相关治疗靶点;也能够研究虫媒病毒的传播防治,从而应用于传染病防控。因而,本人的系列研究具有很强的现实和科学意义。未来本人也将进一步利用上述两个系统,解决天然免疫信号跨器官传递与病毒感染的互作关系。
蚊子等昆虫感染内共生菌Wolbachia可获得强效的抗病毒能力,且该能力可通过母系传播的方式传递给子代。利用这两项生物学特性,World Mosquito Program在印度尼西亚、斐济和厄瓜多尔等多大洲多国家释放了超过百万只Wolbachia+蚊子,有效的阻断了当地包括登革热、寨卡和西尼罗河热等虫媒病毒的传播,部分地区疫病感染率下降了超过80%。病毒能否突破Wolbachia的保护效应?是否会在选择压力下进化出超级病毒?因此,解析Wolbachia/宿主/病毒三者的共进化,对于评估WMP项目的安全性具有重要的现实意义。目前,我们建立了X病毒/Wolbachia/宿主的代纪进化体系,欢迎对该项目感兴趣的同学加入(图2)。
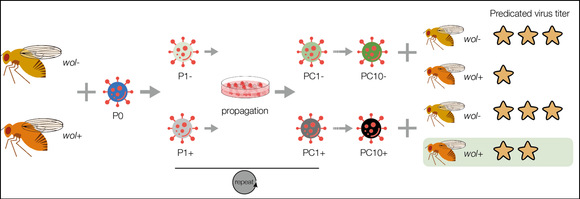
图2 解析Zika/Wolbachia/宿主共进化
三、解析发育信号“外胚层-肌肉”传递的分子机制和调控网络
信号跨器官传递(ICN),不仅局限于免疫系统,其也参与调控其它生物学过程。例如,肌肉发育会依次经历细胞的增值、分化以及形态发生。肌细胞的形态发生,即形成特定细胞形态的过程,是其构成正常组织结构,完成特定生理功能的必备步骤。目前对肌肉细胞增殖和分化的理论机制的阐述已经非常完善,但对肌肉细胞如何正确组织,并构成具有完备功能的肌肉系统的过程却知之甚少。研究表明,肌肉的形态发生障碍,是多种遗传性肌肉疾病的致病原因。因此,临床上对研究肌肉的形态发生机制,提出了迫切的需求。果蝇胚胎期肌肉系统,在12小时内可以迅速完成从增殖、分化到形态发生的完整过程,并最终构成由30种形态各异的肌肉所组成的特定的精细结构,因而非常适用解答前述问题。借助于本人构建的完善的正向遗传学筛选、特定肌肉标记、以及活体肌肉形态追踪等手段,本人发现,肌肉系统的形成是一个受到外源信号和内源信号双重调节的精细过程(图3,通路③和④)。
本人的研究结果表明,在果蝇胚胎期,中胚层肌肉细胞中成纤维生长因子通路(Fibroblast Growth Factor,FGF)组分高度富集,并参与调控肌肉的形态发生。FGF通路受体Heatless和转导分子Stumps缺陷型果蝇均呈现出了典型的肌肉形态发生障碍。而进一步的研究表明,中胚层内肌肉细胞的FGF通路,受到来源于外胚层(表皮/神经)分泌的配体Ths/Pyr的调控。Ths/Pyr通过与肌肉细胞FGF受体Heatless结合,调节下游Pbl/Rho/Rac GTPases通路,从而最终影响细胞骨架以及细胞定向(图3,通路③,Development, 2020)。该研究解析了发育信号“外胚层-肌肉”跨器官调控的分子基础,并对先天性肌肉疾病的诊断和治疗,提出了新的机制和思路。该研究被The Node转载并报道,并获得了2021年度美国遗传学会Drosophila Image Award优秀奖。
在该研究的基础上,本人发现,肌肉细胞的形态发生,不仅受到空间上的外源信号调控,也受到内源激酶的时间性调控(Nature Communications, 2022)。此研究表明,在胚胎发育早期,AurB通过激活包括Polo在内的有丝分裂相关蛋白,调控和促进肌肉细胞的增殖。随着肌肉细胞增殖和分化的完成,该激酶在肌肉组织中选择性沉默,肌肉细胞也进入终末分化状态。AurB在仍然旺盛分裂的神经系统中则仍保持高表达状态。紧接着,随着肌肉细胞形态发生的开始,Bsd在肌肉内表达显著上升,并在该组织内取代AurB的功能,特异性激活Polo,接管Tum/Pav/r-tubulin有丝分裂元件,从而在维持肌肉细胞终末分化状态的前提下,调控细胞的形态发生和肌肉系统的构成(图3,通路④)。整个过程在不同物种中高度保守:Bsd哺乳动物同源蛋白VRK3,在小鼠和人类中均可结合并磷酸化Polo同源蛋白Plk1;敲低VRK3或药物抑制Plk1活性,均可造成肌肉形态发生的障碍;在Bsd突变果蝇背景下,回补其哺乳动物同源基因VRK3,则可有效的拯救表型。该研究的创新之处在于,指出了增殖/形态发生两种完全不同的生物学过程,不仅由同一个元件所介导,且阐明了其核心为上游调控性激酶的时空性和特异性表达。该研究展示了生命体是如何化繁为简,利用有限的元件,高效的完成不同生命过程。更进一步,此研究总结了肌肉形态发生的内源性和外源性调控机制,提出转录因子Jumu同时调节heartless和bsd的表达(图3 通路⑤),从而将外源性信号和内源性信号纳于同一个调控体系之下,完整的解释了肌肉形态发生的生物学机制,并验证了果蝇体系可以有效的研究高等动物肌肉形态发生的问题 (Developmental Biology, 2023)。
在此基础上,通过与临床医生合作,本人成功构建了线状体肌病(Nemaline Myopathy)的体内研究模型,并证明了果蝇/斑马鱼模型可以有效的预测人类TPM2蛋白突变的致病性,以及其所诱发的先天性线状体肌病的严重程度(图3 通路⑥)。该研究对于优生优育和产后手术干预,提出坚实的理论和实验基础(JCI insight, 2022)。
Migraosome是近年来新发现的细胞器,其在细胞迁移、定位以及器官发育过程中具有重要功能。未来,我们将利用果蝇胚胎模型探索Tsp5D是否参与肌肉细胞的形态发生,欢迎有兴趣的同学参与该项研究。
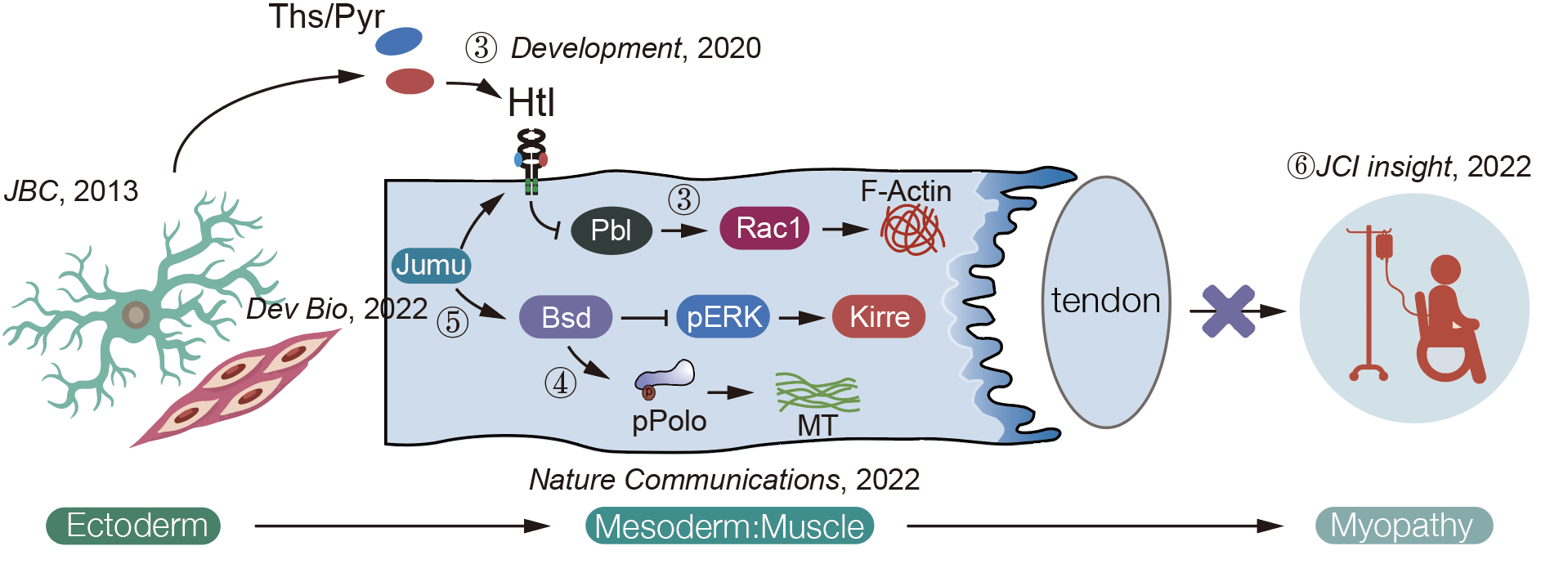
图3 肌肉发育的双重调控网络
四、解析神经炎症诱发的肌无力的分子机制
感染和神经退行性疾病,不仅能在中枢神经系统中诱发包括神经炎症在内的“脑”相关症状,也能导致包括肌无力、肌肉疼痛和肌肉疲劳在内的“肌肉”相关症状。我们通过建立三种研究模型(细菌性脑炎、病毒性脑炎、阿尔茨海默症),系统性探究了神经炎症诱发肌肉疾病的分子机制。
研究表明,感染/神经退行性疾病均可导ROS在脑组织中的堆积,过量的ROS可诱导炎症因子IL-6 (Upd3)的表达。神经来源的IL-6 /Upd3可穿透血脑屏障,进入循环系统,从而激活肌肉JAK/STAT通路,最终影响肌肉中线粒体功能和肌肉表现(图4 通路⑦)。
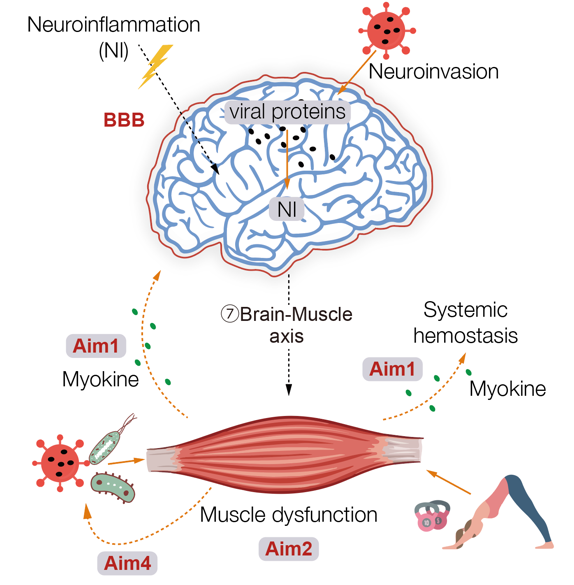
图4 “大脑-肌肉”交互作用网络
我们的研究首次发现了中枢神经系统可通过非神经连接体(Connectome)方式,直接影响肌肉生理功能,并鉴定出Upd3/IL-6蛋白作为ICN分子,参与“大脑-肌肉”交流,从而为针对性开发统一药物提供了理论基础。未来,我们将进一步探索JAK/STAT通路影响线粒体功能的具体分子机制,欢迎有兴趣的同学参与该项研究。
五、运动/阿尔茨海默症/肌肉互作
临床证据显示,运动对AD进程具有明显的抑制作用,其机理可能是抑制脑中Aβ蛋白的积累、Tau蛋白的表达和神经纠缠节(Neurofibrillary tangles, NFT)的形成。较之于表型,肌肉跨器官调节大脑生理状态的分子基础,仍有待解析。
肌肉因子(Myokine),即肌肉来源的分泌性蛋白,是一类重要的ICN分子(图4)。感染、胁迫以及损伤等多种刺激均可诱发肌肉生理状态的变化,影响肌肉因子的表达谱和分泌谱。肌肉作为运动器官,其响应运动的肌肉因子,被称为运动响应肌肉因子(Exercise Responsive Myokines, ERM),具有尤为特殊的调控效能。近些年的研究表明,ERM作为ICN分子参与调节大脑生理状态。例如,肌肉分泌的转硒蛋白可以改善脑中海马体损伤和衰老导致的认知障碍。运动所促进的Irisin生成和分泌,则可通过“肌肉-大脑”轴影响AD进程。鉴于其功能,这些ERM又被称为神经保护性ERM(Neuro Protective ERM, NPERM)。NPERM在AD防治中具有突出的理论优势。目前的研究痛点为,NPERM造成的副作用,例如Irisin对代谢的不良影响,制约了其临床转化应用。
综上,研究运动保护作用的机制,深入探索ERM/AD的相互作用,模拟运动效应,认识不同器官之间的协同作用,进而寻找更为高效的神经保护性肌肉因子NPERM,针对普遍缺乏运动能力或者运动意愿老年人,制定有效缓解和防治AD的临床应用措施,具有重要的现实价值。本课题组将建立果蝇-斑马鱼-小鼠三级筛选体系,寻找新型NPERM,并通过积极与临床医生合作,寻求转化应用(图5)。
综上所述,本人的研究,聚焦于信号跨器官传递(ICN),解析并阐明了天然免疫信号的“肠-肝”传递机制,肌肉形态发生的双重调控网络,以及IL-6介导的“大脑-肌肉”调控路径。同时,本人的研究不仅致力于解决基础生物学问题,更积极结合社会迫切的现实需求,响应用科学知识切实服务社会的号召,着重推进遗传学导向的转化医学。本人未来的研究将聚焦于揭示ICN对包括阿尔茨海默症以及病毒感染在内的多种疾病进程的影响,并开发相应干预措施。
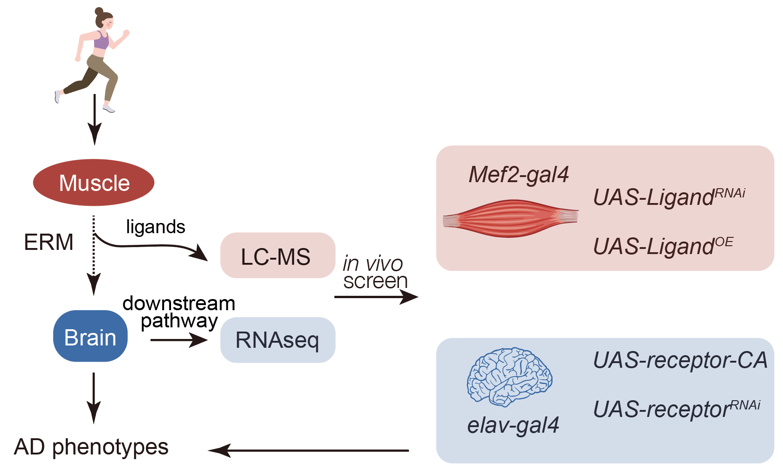
图5 筛选AD效应性NPERM
个人简介
2018年9月至2023年1月,在Washington University(WUSTL)与Aaron Johnson教授合作从事博士后研究。2023年2月入职幸福宝导航app入口,研究方向主要集中于信号跨器官传递、肌肉形态发生以及疾病建模等领域,以第一作者身份在Cell Host&Microbe, Nature Communications, JCI insight, Development, Journal of Virology, Developmental Biology等期刊发表多篇论文。实验室目前主要关注于三个方向:第一,探索多器官互作网络在整体稳态中的功能和机制;第二,筛选针对阿尔茨海默症的运动保护性因子;第三,解析肌肉细胞形态发生的调控因子。实验室目前和清华大学医学院,中国农业科学院哈尔滨兽医研究所,University of Florida School of Medicine,Washington University School of Medicine等单位建立了稳定的合作关系。实验室目前有硕士生一人、博士生两人以及博士后一人(获得2023年度上海市超级博士后资助)。欢迎感兴趣的同学加入。
招生专业:
细胞生物学、发育生物学
科研项目:
国家自然科学基金优秀青年基金(海外), 国家自然科学基金委/中共中央组织部, 2022
获奖情况:
中国科学院研究生科技创新与社会实践资助专项, 中国科学院, 2013.
Disease Models & Mechanisms Conference Travel Grant, The Company of Biologists Ltd, 2020.
2021 Drosophila Image Award, Drosophila Image Award Committee, sponsored by Genetics Society of America, 2021
上海市领军人才(海外), 上海市政府, 2022
代表性论文和论著:
1、Infection and chronic disease activate a brain-muscle signaling axis that regulates muscle performance
Yang, S., Tian, M.,Yamada, S., Wang, Y., Feng, S., Chhangani, D, Ou, T., Li, W., Yang, Z., McAdow, J., Rincon-Limas. D., Yin, X., Tai, W., Cheng, G., and Johnson, A..
In Revise.
2、An in vivo platform to identify clinically relevant pathogenic loci using Drosophila melanogaster
Yamada, S., Ou, T., Nachadalingam, S., Yang, S.#, Johnson, A.#.
#Corresponding author
DOI: https://doi.org/10.1101/2023.11.01.565153
In Revise.
3、The serine/threonine kinase Back seat driver prevents cell fusion to maintain cell identity
Yang, S., Johnson, A.
Developmental Biology. 2023 Mar 14; 495:35-41. [PMID: 36528051]. IF: 3.15
2022
4、A pathogenic mechanism associated with myopathies and structural birth defects involves TPM2 directed myogenesis
McAdow, J.#, Yang, S.#, Ou, T., Huang, G., Dobbs, M., Gurnett, C., Greenberg, M., Johnson, A.# co-first author.
JCI insight. 2022 May 17; 7(12):e152466. [PMID: 35579956]. IF: 9.484
5、Spatiotemporal expression of regulatory kinases directs the transition from mitotic growth to cellular morphogenesis in Drosophila
Yang, S., McAdow, J., Du, Y., Trigg, J., Taghert P., Johnson, A.
Nature Communications. 2022 Feb 9;13(1):772. [PMID: 35140224]. IF: 17.694
2020
6、FGF signals direct myotube guidance by regulating Rac activity
Yang, S., Week, A., Du Y., Valera, J, Jones, K., Johnson, A.
Development, 2020 Feb 7;147(3):dev183624. [PMID: 31932350]. IF: 6.862
2019
7、Sugar alcohols of polyol pathway serve as alarmins to mediate local-systemic innate immune communication in Drosophila
Yang, S., Zhao, Y., Yu, J., Fan, Z., Gong, S., Tang, H, L., Pan, L.
Cell Host & Microbe, 2019 Aug 14;26(2):240-251.e8. [PMID: 31350199]. IF: 31.316
8、Establishment of viral infection and analysis of host-virus interaction in Drosophila melanogaster
Yang, S., Zhao, Y., Yu, J., Fan, Z., Gong, S., Tang, H, L., Pan, L.
Journal of Visualized Experiments, 2019 Mar 14;(145). [PMID: 30933079]. IF: 1.424
2018
9、Bub1 facilitates virus entry through endocytosis in the model of Drosophila pathogenesis
Yang, S., Yu, J., Fan, Z., Gong, S., Tang, H, L., Pan, L.
Journal of Virology, 2018 Jul 5, 92(18), e00254-18. [PMID: 29976667]. IF: 6.549
10、Macrophage-derived IL-1 alpha promotes sterile inflammation in a mouse model of acetaminophen hepatotoxicity
Zhang, C., Feng, J., Du, J., Zhuo, Z., Yang, S., Zhang, W. Wang, W. Zhang, S. Iwakura, Y. Meng, G. Fu, Y. X. Hou, B. Tang, H.
Cellular & Molecular Immunology, 2018 Nov;15(11):973-982. [PMID: 28504245]. IF: 22.096
2017
11、Bap180/Baf180 is required to maintain homeostasis of intestinal innate immune response in Drosophila and mice
He, X., Yu, J., Wang, M., Cheng, Y., Han, Y., Yang, S., Shi, G., Sun, L., Fang, Y., Gong, S.T., Wang, Z., Fu, Y.X., Pan, L. & Tang, H.
Nature Microbiology, 2017 Apr 18;2:17056, [PMID: 28418397]. IF: 30.964
2013
12、Myotubularin-related protein 4 (MTMR4) attenuates BMP/Dpp signaling by dephosphorylation of Smad proteins
Yu, J., He, X., Chen, Y.G., Hao, Y., Yang, S., Wang, L., Pan, L. & Tang, H.
Journal of Biological Chemistry, 2013 Jan 4; 288(1): 79–88, [PMID: 23150675]. IF: 5.486

